Neoplasie maligne e benigne

Neoplasie maligne e benigne
Tumori Oculari Benigni:
EMANGIOMA
DELLA COROIDE
Il
più frequente tumore primitivo vascolare della coroide è l’emangioma
cavernoso circoscritto. Gli altri tumori vascolari primitivi della coroide (l’emangiopercitoma
e l’emangioma capillare) sono estremamente rari.
L’emangioma cavernoso coroideale può essere di tipo circoscritto o diffuso.
Quest’ultima forma può essere correlata alla Sindrome di Sturge-Weber.
L’EMANGIOMA
COROIDEALE CIRCOSCRITTO
Definizione
e classificazione
L’emangioma coroideale circoscritto è un importante tumore vascolare
che entra in diagnosi differenziale con altre lesioni amelanotiche dell’uvea
(melanoma amelanotico, metastasi, osteoma, degenerazione maculare ecc.).
La forma circoscritta di questo tumore
benigno è raramente associata al nevus flammeus cutaneo che invece caratterizza
la sindrome di Sturge-Weber.
La frequenza di questo tumore, di solito unilaterale, è di circa 30
volte inferiore rispetto a quella del melanoma uveale anche perché molti casi,
essendo asintomatici, rimangono misconosciuti.
Caratteristiche
cliniche e diagnostiche
Il
tumore rimane generalmente misconosciuto fino a quando diventa sintomatico. La
comparsa di sintomi, calo dell’acuità visiva e/o metamorfopsie, avviene
generalmente nella terza o quarta decade di vita.
L’esame obiettivo del segmento anteriore è sempre normale così come la
pressione intraoculare.
Oftalmoscopicamente il tumore appare come una massa sottoretinica di un colore
rosso arancio spesso identico a quello della coroide circostante. Sulla
superficie tumorale possiamo ritrovare foci bianco-giallastri o più
frequentemente accumuli di pigmento sottoretinico a livello di epitelio
pigmentato retinico.
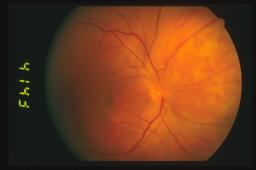
La
dimensione dell’emangioma coroideale varia circa da tre a 18 mm di diametro
massimo e da uno a 7 mm di spessore.
La sede più frequente di riscontro dell’emangioma coroideale è la coroide
posteriore. In particolare l’80% ha sede al polo posteriore ed il rimanente
20% è in genere parapapillare.
La presenza di un emangioma in sede sottomaculare determina già nei primi anni
di vita un'ipermetropia monolaterale con rischio d'ambliopia. Queste
caratteristiche devono quindi far sospettare, nelle ambliopie anisometropiche
dell’infanzia, la presenza di un emangioma corideale sottomaculare.
Se il tumore è invece paramaculare, si potrà avere un calo dell’acuità
visiva in età adulta dovuto ad un sollevamento sieroso del neuroepitelio
retinico coinvolgente la fovea. Nell’adulto, alla presenza di distacchi
sierosi del neuroepitelio al polo posteriore, deve essere quindi esclusa la
presenza di piccoli emangiomi coroideali paramaculari.
Quando il distacco del neuroepitelio persiste per
lungo tempo si potranno osservare alterazioni atrofiche dell'epitelio pigmentato
retinico (“sindrome gravitazionale”), degenerazioni cistiche ingravescenti
della retina e zone ischemiche retiniche periferiche con neovasi retinici al
loro margine. In presenza di tumori di grosse dimensioni si possono avere
distacchi retinici secondari totali.
In genere l’emangioma coroideale ha delle caratteristiche oftalmoscopiche tali
da consentire una diagnosi agevole.
Esistono
tuttavia delle lesioni d'aspetto morfologico non caratteristico che rendono
difficile la diagnosi differenziale con altre lesioni amelanotiche coroideali
(melanoma amelanotico, metastasi, corioretinopatia sierosa centrale, sclerite
posteriore, osteoma della coroide, degenerazione maculare senile, ecc.). In
questi casi, oltre alla valutazione oftalmoscopica binoculare diretta o
indiretta (Infatti è fondamentale la visione stereoscopica del fondo oculare
che permette di visualizzare la “rilevatezza” del tumore sul piano retinico
ed il suo colore.), è necessario eseguire alcuni esami strumentali aggiuntivi.
Per
una corretta interpretazione delle immagini diagnostiche ricavabili da indagini
strumentali bisogna tenere sempre presente la sede coroideale del tumore e le
sue caratteristiche istologiche. Infatti, l’emangioma è costituito da un
gomitolo di vasi sanguigni con scarsissimo tessuto di sostegno perivascolare in
cui vi è un flusso ematico rapido e vorticoso di molto superiore alla coroide
sana circostante.
Gli esami strumentali in grado di dare immagini
patognomoniche d'emangioma coroideale sono l’ecografia Ad e B Scan e
l’angiografia con verde indocianina.
L’ecografia A-scan standardizzata mostra picchi acustici intralesionali ad
alta reflettività pari a circa l’80-90% del picco retinico di apertura.
Quest'alta reflettività interna, è patognomonica di emangioma coroideale, ed
è determinata dalle numerose interfacie acustiche che costituiscono le pareti
dei vasi dell’emangioma.
In B-scan, l’emangioma mostra sempre una forma ovalare a volte associata
all’immagine di un piccolo distacco del neuroepitelio sovrastante il tumore o
di un sollevamento sieroso retinico più ampio perilesionale. L’immagine è ad
alta reflettività paragonabile a quella del grasso retrobulbare e superiore a
quella della coroide circostante.Il tumore non invade mai la membrana di Bruch e
quindi, immagini a forma di fungo, sono sempre patognomoniche
di melanoma coroideale. L’immagine ecografica di calcificazioni intralesionali
è talvolta visibile nel contesto di un emangioma coroideale. Tali lesioni sono
però facilmente distinguibili dall’aspetto ecografico d'iperiflettività
assoluta dell’osteoma coroideale.
Un altro esame fondamentale, nella diagnosi differenziale
tra emangioma e lesioni amelanotiche della coroide, è l’angiografia con verde
indocianina che permette di visualizzare la circolazione della coroide e dei
tumori coroideali non pigmentati.
Nell’emangioma coroideale, l’angiografia con verde indocianina mostrerà un
rapido riempimento del tumore (iperfluorescenza precoce), dovuto al flusso
ematico intenso, con un'iperfluorescenza
massima dopo circa 30 sec.
Dopo
tale periodo vi è un altrettanto rapido svuotamento dei vasi tumorali dal
colorante con un'ipofluorescenza del tumore rispetto alla coroide circostante.
Infatti, la scarsità di tessuto di sostegno perivascolare dell’emangioma,
determina un ridotto accumulo di colorante rispetto alla coroide sana
circostante.
Invece nelle altre lesioni amelanotiche tumorali o pseudotumorali l’elevata
quantità di tessuto rispetto all’esigua vascolarizzazione interna determinano
nell’angiografia con verde indocianina un lento riempimento iniziale
(ipofluorescenza precoce) e un accumulo maggiore di colorante in sede
extravasale nelle fasi tardive (iperfluorescenze tardive) dell’esame.
Altri
esami strumentali utili nella gestione dell’emangioma coroideale sono
l’angiografia a fluorescenza e la tomografia coerente a radiazioni ottiche (OCT).
Queste indagini strumentali, pur non fornendo informazioni patognomoniche,
consentono una valutazione qualitativa e quantitativa delle alterzioni retiniche
secondarie alla presenza del tumore o agli esiti del suo trattamento.
L’angiografia a fluorescenza permette una
visualizzazione del distacco sieroso del neuroepitelio, che determina il calo
dell’acuità visiva, e la scoperta di una lesione coroideale adiacente o
sottostante.
Inoltre le alterazioni atrofiche “gravitazionali” dell’epitelio pigmentato
retinico sono ben visibili all’angiografia e dimostrano che la lesione è
datata.
L’OCT è un’indagine strumentale, di
recente introduzione, che ci consente un rapido e non invasivo studio degli
strati retinici in senso qualitativo e quantitativo. L’esame consente di
evidenziare e quantificare il sollevamento del neuroepitelio maculare secondario
all’emangioma coroideale. Tali parametri saranno quindi monitorati nel tempo
per valutare follow-up naturale o dopo trattamento.
Istopatologia
Alla
valutazione istologica il tumore appare come una massa di vasi sanguigni
congesti. Possono essere prevalentemente di tipo capillare, cavernoso o misti.
La forma cavernosa è la più frequenter ed è caratterizzata da ampi vasi
congesti separati da sottili setti connettivali. La forma capillare è rara ed
è costituita da fini capillari separati da connettivo. Le alterazioni della
retina soprastante il tumore sono caratterizzate da degenerazioni cistiche
retiniche, macrofagi contenenti melanina o lipofuscina, metaplasie
dell’epitelio pigmentato retinico.
Trattamento
L’emangioma
della coroide è un tumore benigno e quindi il trattamento non è finalizzato
alla distruzione del tumore a qualsiasi costo ma, invece, al mantenimento della
migliore acuità visiva per il maggior tempo possibile.
Se il paziente non ha sintomi o calo dell’acuità visiva il trattamento non è
necessario ed il paziente andrà controllato nel tempo.
Se un sollevamento del neuroepitelio determina un calo dell’acuità visiva il
trattamento dovrà essere preso in considerazione.
I trattamenti sono essenzialmente di due tipi: la laser terapia e la
radioterapia.
La scelta della migliore terapia per un determinato emangioma dipende dal suo
spessore, dal diametro, dall’ampiezza del sollevamento sieroso del
neuroepitelio, dalla presenza di danni irreversibili retinici maculari e dalla
localizzazione del tumore.
Lo
scopo del trattamento fotocoagulativo laser è di creare, sopra la superficie
tumorale, delle cicatrici retino-coroideali tali da consentire creare
un'adesione della retina all’epitelio pigmentato sottostante allo scopo di
ridurre l’essudazione con una conseguente diminuzione o scomparsa del
sollevamento sieroso del neuroepitelio ed un miglioramento dell’acuità
visiva.
Questo tipo d'approccio terapeutico è indicato per emangiomi di piccole e medie
dimensioni. La fotocoagulazione può essere intensa con spot confluenti sulla
superficie del tumore oppure con spot intensi ma radi sulla superficie tumorale.
Quest’ultima opzione è consigliabile per le lesioni paramaculari.
L’angiografia
a fluorescenza consente un utile monitoraggio degli esiti del trattamento laser.
Un nuovo approccio terapeutico mediante laser a diodo è la Termo Terapia
Transpupillare (TTT). Questo trattamento, attualmente utilizzato con successo
nella distruzione di melanomi coroideali di piccole dimensioni, è stato
eseguito in via sperimentale anche nell’emangioma coroideale.
Il trattamento alternativo al laser è la radioterapia a basse dosi eseguibile
con diversi approcci, radioterapia esterna, placche episclerali, protoni e gamma
knife. Questo trattamento determina nel tempo una distruzione dell’emangioma
con una risoluzione del distacco retinico secondario.
Le indicazioni per l’utilizzo della radioterapia
riguardano le lesioni sottomaculari con sollevamento retinico e gli emangiomi di
grandi dimensioni.
La prognosi quoad vitam è eccellente essendo l’emangioma un tumore benigno.
La prognosi visiva dipende dalla sede, dall’ampiezza della lesione e
soprattutto dalla presenza, dall’estensione e dalla durata del sollevamento
del neuroepitelio maculare.
EMANGIOMA
COROIDEALE DIFFUSO
L’emangioma
coroideale diffuso è un tumore benigno vascolare occupante la coroide
posteriore che si continua con la coroide circostante con margini mal definiti.
L’emangioma coroideale diffuso è presente nel 50% dei pazienti con la
sindrome di Sturge Weber ma può essere presente, seppur raramente, da solo.
A differenza della forma circoscritta, quest'emangioma è generalmente
diagnosticato nella prima decade di vita a causa dell’ambliopia ipermetropica
che determina o per la presenza dell’emangioma cutaneo.
La
pupilla dell’occhio affetto ha un riflesso più rosso del controlaterale sano
mentre vitreo e cristallino sono trasparenti. Oftalmoscopicamente si apprezza un
diffuso ispessimento coroideale rossastro che meglio si evidenzia all’esame
ecografico in B-Scan.
La
gestione dell’emangioma coroideale diffuso è difficile a causa delle
dimensioni dell’emangioma e si basa sulla fotocoagulazione, la radioterapia o
la chirurgia.
Inoltre molto frequentemente nell’occhio affetto da emangioma è presente un
glaucoma cronico ad angolo aperto.
La prognosi visiva è scarsa e la prognosi quoad vitam appare condizionata solo
se l’emangioma oculo-cutaneo è associato ad un emangioma leptomeningeo
diffuso (Sindrome di Sturge Weber).
EMANGIOMA CAPILLARE
L’emangioma
capillare della coroide è una variante istopatologica dell’emangioma
coroideale circoscritto. La lesione è costituita, contrariamente ai grossi vasi
dilatati coroideali dell’emangioma circoscritto, da vasi di piccole
dimensioni.
In
alcuni casi è associato ad emangiomi capillari cutanei
EMANGIOPERCITOMA
UVEALE
Si tratta di un tumore rarissimo di cui sono riportati pochi casi in letteratura. L’emangiopercitoma è costituito da una proliferazione di periciti vascolari. L’aspetto oftalmoscopico è quello di un tumore coroideale amelanotico. L’angiografia e l’ecografia oculare non danno immagini patognomoniche della lesione. Istologicamente si tratta di un agglomerato di canali vascolari separati da tessuto costituito da periciti.
L’emangioma
capillare si può presentare come una lesione solitaria retinica, o può far
parte della sindrome di von Hippel-Lindau in cui sono associate angiomatosi
sistemiche.
Tuttavia in entrambi i casi il tumore appare clinicamente e istologicamente
identico.
Definizione e classificazione
di cellule endoteliali e canali vascolari. La lesione è diagnosticata in
genere tra i 10 ed i 30
anni quando la lesione, essudando, determina un calo dell’acuità visiva. La
lesione può essere multipla nel 30% dei casi.
La bilateralità e la molteplicità delle lesioni implicano una mutazione
genetica e l’appartenenza alla sindrome di von Hippel Lindau.
Caratteristiche
cliniche e diagnostiche
Nello
stadio precoce, l’emangioma periferico è molto piccolo e
oftalmoscopicamente lo s'individua a fatica ma lo si può localizzare più
agevolmente seguendo i vasi afferenti ed efferenti dilatati. Quando il tumore
s'ingrandisce appare un nodulo rosso-rosa con i caratteristici vasi afferenti
ed efferenti dilatati che arrivano fino alla papilla ottica.
Se il tumore è invece in sede epipapillare o iuxtapapillare può apparire
come un nodulo a margini netti senza i vasi dilatati.
L’emangioma capillare retinico può essere diviso nella forma essudativa e
vitreoretinica.
La forma essudativa è caratterizzata da
un'essudazione intraretinica e sottoretinica che inizialmente è
perilesinale e successivamente alla crescita del
tumore aumenta fino a coinvolgere la macula. Nei casi più avanzati
l’essudazione può determinare anche un distacco retinico essudativo totale
simile a quello della malattia di Coats.
La forma vitreoretinica è invece
caratterizzata da emangiomi retinici con minima reazione essudativa ma con una
reazione vitreale intensa che può determinare la formazione di bande vitreali
e quindi trazione vitreo retinica. Queste trazioni possono determinare
distacchi di retina trazionali ed evolvere in ptsi bulbare.
L’emangioma capillare retinico periferico ha un aspetto oftalmoscopico
caratteristico. In presenza di una vasta essudazione retinica coinvolgente il
polo posteriore il tumore entra in diagnosi differenziale con la malattia di
Coats da cui tuttavia si differenzia per la presenza costante del tumore e dei
vasi dilatati.
Altre lesioni con cui entra in diagnosi differenziale
l’emangioma capillare retinico sono l’emangioma racemoso retinico, l’emangioma
cavernoso retinico, i macroaneurimi retinici con essudazione ecc.
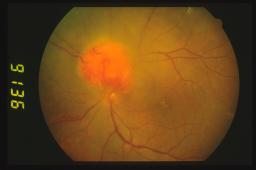
L’emangioma
in sede peripapillare può entrare in diagnosi differenziale con il
papilledema e con la papillite. Un accurata anamnesi, un’attenta
oftalmoscopia binoculare ed un’angiografia a fluorescenza sono in grado di
differenziare le lesioni.
Tra gli esami strumentali la fluorangiografia
consente di valutare dinamicamente il riempimento e lo svuotamento dei vasi
afferenti ed efferenti e di rivelare la presenza di altre lesioni di
piccole dimensioni e misconosciute all’esame oftalmoscopico. L’esame è
inoltre una guida indispensabile al trattamento laser dell’emangioma ed al
suo follow-up.
L’ecografia
oculare e l’angiografia con verde indocianina non danno informazioni
aggiuntive di particolare interesse clinico nella diagnostica differenziale.
L’emangioma retinico consiste in una proliferazione di
capillari che sostituiscono a tutto spessore la retina. La crescita può
avvenire verso il vitreo (endofitico) o verso la coroide (esofitico). La
proliferazione benigna riguarda le cellule endoteliali ed i periciti.
All’interno del tumore può esistere una marcata proliferazione fibrogliale.
Il
trattamento deve iniziare solo quando il tumore, mostrando segni di crescita,
aumenterà l’essudazione retinica. Se non cresce e non determina essudazione
retinica deve essere controllato oftalmoscopicamente ogni 3-4 mesi.
I trattamenti dipendono dalla sede, dimensioni del tumore, dalla trasparenza
dei mezzi diottrici e dal grado di fibrosi vitreoretinica.
Lo scopo del trattamento di questo tumore benigno, ma a crescita lenta, è la
sua distruzione per fermare l’essudazione intra e sottoretinica maculare che
è la causa del calo dell’acuità visiva.
Il trattamento fotocoagulativo laser
transpupillare viene eseguito prevalentemente su tumori periferici di piccole
e medie dimensioni. La tecnica utilizzata consiste nell’utilizzare basse
potenze e lunghi tempi di esposizione.
Il trattamento sarà diretto sul tumore ed in un’unica
sessione per gli emangiomi di piccole
dimensioni (< a un diametro papillare).
Per gli emangiomi di diametro maggiore più
grandi si preferisce iniziare con un trattamento perilesionale
(doppia fila di spot) e dopo trenta giorni circa si esegue il trattamento sul
vaso afferente. Successivamente si tratterà direttamente la massa tumorale
fino alla sua completa distruzione (fig.5).
Negli emangiomi periferici più grossi, è consigliabile utilizzare la
crioterapia con la tecnica del triplo congelamento ed eventualmente ripetere
il trattamento a distanza di tre mesi.
Il successo del trattamento comporterà una scomparsa degli essudati retinici
ed anche
riduzione del calibro della forma dei vasi retinici tumorali.
EMANGIOMA
CAVERNOSO RETINICO
Emangioma
cavernoso retinico è un tumore vascolare benigno. Lo si diagnostica più
frequentemente nei giovani adulti come lesione solitaria oculare o associata
ad altre malformazioni cutanee ed intracraniche.
Oftalmoscopicamente appare come un grappolo di aneurismi di colore rosso scuro
generalmente nella retina periferica e più raramente vicino al disco ottico.
A differenza dell’emangioma capillare retinico le pareti vascolari non sono
alterate e quindi viene a mancare la componente essudativa perilesionale.
Istologicamente si tratta infatti di vene retiniche dilatate e congeste.
Alla fluorangiografia retinica i vasi rimangono ipofluorescenti nelle fasi
precoci e solo nelle fasi tardive gli aneurismi si riempiono di colorante.
Nella maggior parte dei casi non è necessaria alcuna terapia ed il riscontro
del tumore vascolare è spesso casuale. In rari casi vi può essere
un'emorragia vitreale e tale complicanza può richiedere una terapia adeguata
chirurgica e/o laser.
EMANGIOMA
RACEMOSO RETINICO
L’emangioma
racemoso o cirsoide retinico è un’imponente alterazione vascolare del
circolo retinico dovuta
ad un’anastomosi diretta arteria-vena.
La valutazione oftalmoscopica mostra un caratteristico ammasso di vasi
tortuosi, congesti e dilatati a partenza dalla papilla ottica.
Alla fluorangiografia si dimostra la comunicazione arteria-vena con un rapido
riempimento del tumore ma senza accumulo di colorante o essudazione.
L’evoluzione è molto lenta con complicanze oculari rare (emorragie
retiniche o occlusioni vascolari).
L’emangioma racemoso può essere una componente della sindrome di
Wyburn-Mason per cui il paziente
deve essere indagato per escludere la presenza di queste alterazioni vascolari
in altre parti del corpo (cervello, orbita, mandibola ecc.).
TUMORE
VASOPROLIFERATIVO DEL FONDO OCULARE
Il
tumore vasoproliferativo del fondo oculare (TVPFO) è una massa rosso-rosa con
vaso retinico afferente e venoso efferente solo
lievemente tortuosi ma non dilatati.
Clinicamente possiamo dividere il tumore in forma primaria e forma secondaria.
La forma primitiva è in genere una lesione solitaria, monolaterale,
localizzata nel quadrante infero temporale.
La forma secondaria occorre in occhi con lesioni predisponenti (uveiti,
toxocariasi, retinite pigmentosa ecc.), bilaterale ed associata ad una forte
essudazione retinica.
La terapia fotocoagulativa laser è riservata a lesioni piccole e con scarsa
essudazione. Per lesioni di grandi dimensioni o con intensa essudazione è
preferibile la crioterapia.
ASTROCITOMA
RETINICO
L’amartoma
astrocitico della retina è un tumore benigno composto da cellule gliali in prevalenza
astrociti.
Clinicamente esistono due forme. La forma solitaria retinica non associata a
sclerosi tuberosa e quella associata a lesioni amartomatose multiple
extraoculari (astrocitoma intracranico, angiofibroma cutaneo, chiazze cutanee
di depigmentazione, rabdomioma cardiaco, angiolipoma renale, ecc.) tipiche
della sclerosi tuberosa.
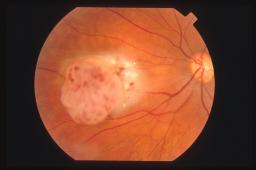
Oftalmoscopicamente
la lesione appare in due forme principali. Una sessile non calcifica ed una
composta da sferule calcifiche che lo fanno entrare in diagnosi differenziale
con il retinoblastoma da cui differisce per la mancanza di feeder vessels.
Fluorangiograficamente si apprezzano i vasi tumorali ed un iperfluorescenza
tardiva. Nei casi più atipici può essere necessario la biopsia mediante ago
aspirato.
TUMORI
MIOGENICI
I
tumori miogenici dell’uvea sono il rabdomiosarcoma ed il leiomioma.
Il rabdomiosarcoma è un tumore maligno mesenchimale dell’infanzia. In letteratura esistono solo tre casi di rabdomiosarcoma dell’iride e dei corpi ciliari. Il tumore è indistinguibile alla valutazione clinico-strumentale da altre neoplasie.
Il leiomioma è un tumore benigno della muscolatura liscia colpisce in genere giovani donne. Clinicamente appare simile ad un melanoma amelanotico con vasi sentinella e con estensione sclerale. Il leiomioma è più frequentemente irideo e solo più raramente si possono trovare grossi tumori dei corpi ciliari a lenta crescita.
La terapia è chirurgica od osservazionale.
TUMORI NEUROGENICI
I tumori neurali che originano nel tratto uveale sono lo schwannoma, il neurofibroma.
Lo schwannoma (neurilemoma) è un tumore benigno delle guaine dei nervi ciliari del tratto uveale. Clinicamente appare come una neoformazione coroideale, prevalentemente non pigmentata, indistinguibile da un melanoma uveale.
Istologicamente è una proliferazione di cellule di Schwann e può presentarsi come forma solitaria o molto più raramente associata alla neurofibromatosi.
Il neurofibroma occorre in genere associato alla neurofibromatosi di von Recklinghausen. Si tratta di un amartoma di cellule gliali e melanocitiche a livello di iride (noduli di Lisch) e a livello di coroide.
Definizione
e Classificazione
L’osteoma
della coroide è un tumore benigno dell'uvea costituito da tessuto osseo. Data
la rarità diquesto tumore non esistono dati epidemiologici consistenti sulla
sua incidenza o prevalenza. Tuttavia dalla valutazione della letteratura
esistente l’osteoma appare più frequente nelle donne giovani (20-30 anni)
senza predilezione di razza. La lesione è unilaterale nel 75-80% dei casi.
Caratteristiche
Cliniche e Diagnostica
Oftalmoscopicamente
l’osteoma appare come una lesione sottoretinica placoide giallo-arancio
contenente accumuli di pigmento marrone. La lesione può essere localizzata in
sede peripapillare o al solo polo posteriore. Le dimensioni variano da alcuni
millimetri di diametro fino ad occupare tutto il polo posteriore. La forma può
essere rotonda od ovoidale con margini ben definiti ma irregolari. Quando il
tumore è bilaterale le dimensioni sono spesso asimmetriche. Sulla superficie
del tumore sono talvolta visibili dei ciuffi di vasi che originano nella parte
profonda del tessuto osseo. In alcuni casi si possono sviluppare, nel contesto
del tumore, delle membrane neovascolari o dei sollevamenti sierosi del
neuroepitelio.
L’aspetto
oftalmoscopico è spesso patognomonico di osteoma coroideale. Tuttavia il
tumore entra in diagnosi differenziale con altre lesioni tumorali o
pseudotumorali della coroide (melanoma amelanotico, metastasi, emangioma,
degenerazione maculare ecc.).
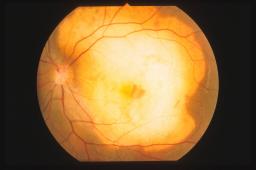
L’ecografia
oculare B-scan è un esame strumentale fondamentale nella diagnosi
differenziale. Permette, infatti, di evidenziare l’alta reflettività del
tessuto osseo tumorale che blocca tutti gli ultrasuoni determinando dietro
alla lesione “ un’ombra acustica”. Riducendo gradualmente la sensibilità
dello strumento permane l’immagine iperriflettente del tessuto osseo mentre
si riduce quella del tessuto adiposo retrobulbare.
La
fluorangiografia retinica permette di visualizzare le alterazioni della
coriocapillare e dell’epitelio pigmentato retinico secondarie alla
sostituzione della coroide da parte del tessuto osseo tumorale. L'esame è
quindi utile nella gestione delle membrane neovascolari sottoretiniche e nei
distacchi sierosi del neuroepitelio retinico.
Molto
più interessante è invece l’aspetto dell’osteoma all’angiografia con
verde indocianina. Quest'esame permette la precisa visualizzazione dei margini
coroideali della lesione e dei ciuffi di vasi che dal profondo del tessuto
osseo risalgono in superficie.
Istopatologia
L’osteoma
è composto di tessuto osseo maturo che sostituisce lo strato coroideale
risparmiando parte della coriocapillare. Nel tessuto tumorale sono presenti le
trabecole ossee contenenti ampi spazi cavernosi ricoperti da endotelio e
piccoli vasi capillari.
Le
linee cellulari presenti sono osteoblasti, osteociti e osteoclasti. Negli
spazi intertrabeculari midollari sono presenti elementi fibrovascolari,
mastcellule e cellule mesenchimali. La coriocapillare appare assottigliata e/o
obliterata ed il sovrastante epitelio pigmentato retinico appare assottigliato
o atrofico contenente accumuli di melanofagi contenenti pigmento.
La
patogenesi di questo tumore è sconosciuta. Sono state ipotizzate diverse
origini (post-infiammatoria, post-traumatica o coristoma) ma le
caratteristiche clinicopatologiche della lesione (tessuto osseo, età
d'insorgenza e progressione) non confermano queste ipotesi.
Essendo
un tumore benigno a lentissima crescita, il trattamento consiste
nell’osservazione periodica e nel monitoraggio delle complicanze che possono
ridurre l’acuità visiva.
Un rapido deterioramento è generalmente legato all’insorgenza di una
membrana sottoretinica maculare. Questa è la complicanza più temibile per la
prognosi visiva e può essere trattata con fotocoagulazione laser secondo
criteri standard.
Un lento deterioramento dell’acuità visiva è invece secondario ad
un'alterazione progressiva dei fotorecettori retinici dovuta all’alterazione
della coriocapillare assottigliata e occlusa dal tumore.
La prognosi visiva dipende quindi anche dalla localizzazione del tumore. Non
esistono invece differenze della prognosi quoad vitam rispetto alla
popolazione normale.
Tumori Maligni
MELANOMA OCULARE
I
melanomi oculari (congiuntivali ed uveali) sono tumori molto rari,
caratterizzati da una prognosi spesso grave. I melanomi uveali
sono spesso asintomatici e determinano disturbi aspecifici
dell’acuità visiva solo quando raggiungono dimensioni ragguardevoli o
interessano l’area maculare. La miglior forma di prevenzione e diagnosi
precoce appare quindi il controllo annuale oftalmologico del fondo oculare.
Il coinvolgimento dell’occhio, organo di piccole dimensioni ma con
funzioni importantissime, impone poi la gestione del paziente presso centri
di alta specializzazione.
Definizione
ed incidenza.
I
tumori maligni congiuntivali sono rappresentati dai carcinomi a cellule
squamose e sebaceo, dal melanoma, dai tumori linfoidi, dal sarcoma di Kaposi.
Tra questi, il melanoma, che origina dai melanociti congiuntivali, è
estremamente raro (meno del 2% di tutti i tumori maligni oculari), con una
incidenza compresa tra 0.024 e 0.052
nuovi casi ogni 100.000 abitanti, pari a circa 1/40 di quella dei melanomi
uveali. La patogenesi di questo tumore è stata sempre fonte di
controversie; attualmente si considera che esso origini nel 75% dei casi da
una melanosi acquisita primitiva (MAP),
mentre nel restante 25% da un nevo congiuntivale pre-esistente o de
novo.
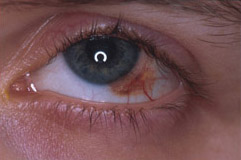
Diagnosi
La
diagnosi differenziale tra melanoma congiuntivale ed altre lesioni
pigmentate benigne (nevo, melanosi, melanocitosi) o pre-cancerose (melanosi
acquisita primitiva) si basa essenzialmente su storia clinica, morfologia
della lesione e reperto bioptico.
Nel nervo congiuntivale esistono spesso spazi cistici intralesionali
comunemente assenti nel melanoma. Inoltre l’incidenza del melanoma è
maggiore nella età di mezzo, mentre è raro nei primi anni di vita e
nell’adolescenza in cui è frequente il riscontro dei nevi. Il melanoma
pigmentato è anche facilmente differenziabile, mediante valutazione al
biomicroscopio, da quelle lesioni a sede sclerale (melanocitosi oculare o
oculodermica) che creano una pseudo pigmentazione congiuntivale.
Tra le lesioni pigmentate della congiuntiva la più importante è la
melanosi acquisita primitiva
(MAP). Si tratta di una lesione piatta, quasi sempre monolaterale, che
colpisce prevalentemente pazienti di media età. Essa può aumentare di
dimensioni o modificare la propria pigmentazione nel tempo, ma, soprattutto,
può trasformarsi in melanoma congiuntivale; questo evento si verifica
50% dei casi di MAP che presentano atipie cellulari all’esame
istologico.
Nelle lesioni con un aspetto morfologico francamente benigno l’approccio
diagnostico si basa sulla valutazione clinica e sulla documentazione
fotografica, ripetute e confrontate nel tempo. Nelle lesioni dubbie di
piccole dimensioni è consigliata l’escissione chirurgica in toto e la
valutazione istologica. Nelle lesioni di maggiore dimensione è preferibile
eseguire biopsie multiple di aree con diversa morfologia. Le biopsie
multiple di lesioni maligne non peggiorano la prognosi.
Il
paziente affetto da melanoma congiuntivale deve essere sottoposto, prima del
trattamento locale, ad indagini diagnostiche per escludere la presenza di
metastasi. Queste possono interessare, per diffusione linfatica, i linfonodi
cervicali, sottomandibolari, preauricolari e addominali, nonché il tessuto
sottocutaneo periorbitario, e, per via ematica, il fegato, lo scheletro, la
parotide ed il sistema nervoso centrale.
Robertson ha riferito su alcuni pazienti con metastasi alle cavità nasali e
paranasali; questa importante segnalazione suggerisce l’esecuzione di una
visita otorinolaringoiatrica.
Trattamento
e risultati
L’approccio
terapeutico è guidato dalle dimensioni e dalla localizzazione del melanoma.
Nei melanomi di piccole dimensioni localizzati in sedi favorevoli
(congiuntiva bulbare e perilimbare) è sufficiente una ampia resezione
chirurgica. Nei casi situati in sedi sfavorevoli (congiuntiva palpebrale,
fornice, caruncola e margine palpebrale) o di grandi dimensioni, l’exenteratio
orbitae, tecnica chirurgica radicale in cui si rimuove tutto il contenuto
orbitario con conseguente cecità e deturpazione del volto, era considerata
l’unico trattamento proponibile.
Un recente studio retrospettivo ha tuttavia dimostrato che la sopravvivenza
dei pazienti sottoposti ad exenteratio orbitae non era migliore di quelli
trattati con exeresi chirurgica locale, suggerendo di limitare l’impiego
della chirurgia radicale ai soli casi che infiltrano l’orbita. Attualmente
nei melanomi a localizzazione sfavorevole si preferisce quindi eseguire
un’asportazione chirurgica totale della lesione con ampio margine di
sicurezza ed associare la crioterapia o la radioterapia.
Quest’ultima utilizza isotopi beta emittenti, quali lo Stronzio-90 ed il
Rutenio-106, che per le loro caratteristiche energetiche, consentono di
somministrare alte dosi a livello della congiuntiva con risparmio del
cristallino (meno del 5% della dose totale).
La mortalità a 5 anni varia dal 14% al 27%; a 10 anni è del 30%
circa. I fattori di rischio statisticamente significativi sulla mortalità
sono la localizzazione sfavorevole (mortalità doppia rispetto alle altre
localizzazioni), la presenza di cellule miste, fusate ed epitelioidi
(mortalità tripla rispetto alla sola cellularità fusata), la multifocalità
(mortalità quintupla rispetto alle forme monofocali). Il grado di invasione
profonda del tumore determina una mortalità più elevata, soprattutto nel
gruppo di pazienti con tumore in sede sfavorevole.
Il melanoma Uveale
Definizione
ed incidenza.
Il
melanoma uveale, che origina dai melanociti uveali della cresta neurale, è il
tumore maligno intraoculare più frequente dell’età adulta; esso tende a
crescere sia all'interno del bulbo, invadendo e disorganizzando i tessuti
intraoculari, sia all'esterno, infiltrando la sclera ed i tessuti orbitari. Il
melanoma uveale metastatizza a distanza unicamente per via ematogena data
l'assenza di vasi linfatici a livello bulbare.
Nel 1979 Wilkes e coll. calcolarono una incidenza annuale nella popolazione
generale di 7 nuovi casi per milione di abitanti, con una grande differenza in
rapporto all’età: tre casi per milione al di sotto dei 50 anni, 21 casi al
di sopra. Attualmente la sua incidenza annuale negli Stati Uniti è stimata
essere di circa 6 nuovi casi per un milione di abitanti. Sulla base di questi
dati possiamo presumere che in Italia si verifichino circa 350 nuovi casi ogni
anno. La sede di insorgenza piu' frequente è la coroide (85%), seguita dai
corpi ciliari (10%) e dall'iride (5%).
Diagnosi
La diagnosi di melanoma coroideale è essenzialmente clinica. La diagnosi differenziale con le altre lesioni pigmentate uveali (nevo, melanocitoma, ipertrofia dell’epitelio pigmentato retinico, emorragia coroideale, neovascolarizzazione, eccetera) si basa sulla valutazione oftalmoscopica da parte di un oftalmologo esperto. Come esami accessori possono essere utilizzati l’angiografia a fluorescenza e/o con verde indocianina e l’ecografia oculare A/B scan.
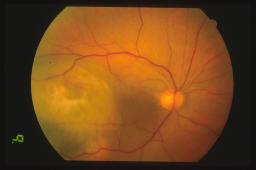
Le
diagnosi differenziali più impegnative riguardano i tumori amelanotici (nevi,
emangiomi, metastasi, osteomi) e quei casi in cui non è possibile
visualizzare la lesione a causa dei mezzi diottrici non trasparenti (lecomi
corneali, cataratta, emovitreo, distacco di retina). In tutti questi casi è
raccomandabile l’uso di metodiche sofisticate quali tomografia
computerizzata, risonanza magnetica nucleare, radioimmuno-scintigrafia o
tomografia ad emissione di positroni. La storia naturale della malattia,
documentata in qualche caso dalla letteratura, è invariabilmente
caratterizzata dallo sviluppo di metastasi a distanza.
Le sedi preferenziali sono il fegato (92% dei casi), il polmone (31%), lo
scheletro (23%), la cute (17%) ed il sistema nervoso centrale (4%). Il tempo
di comparsa dei secondarismi è estremamente variabile (da 2 mesi a 30 anni);
solitamente la loro comparsa porta al decesso entro un anno.
Prognosi
La
classificazione citologica del melanoma uveale è un importante fattore
prognostico. Sono stati identificati tre tipi di cellule: cellule fusate A,
cellule fusate B, cellule epitelioidi. Sulla base di questa suddivisione
Callender classificò i melanomi in 6 gruppi, con prognosi differente: a
cellule fusate A e B, fascicolari, misti, necrotici ed a cellule epitelioidi.
Più recentemente, McLean in un ampio studio retrospettivo ha riclassificato
su base prognostica i melanomi in tre gruppi: nevi a cellule fusate, melanomi
a cellule fusate e melanomi a cellule miste (fusate ed epiteliodi). La
mortalita' a 10 anni variava dallo 0% per i nevi a cellule fusate a più del
50% per i melanomi a cellularità mista. Sono stati individuati altri fattori
in grado di influenzare la prognosi quoad vitam, oltre alla citologia.
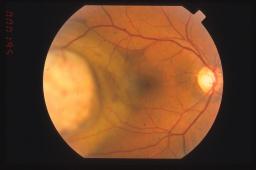
I piu' importanti sono: l'età del paziente, la localizzazione del tumore, il limite del margine tumorale anteriore, il diametro massimo tumorale, l'integrita' della membrana di Bruch e l'infiltrazione sclerale. A titolo puramente esemplificativo si può ritenere che un paziente anziano con un melanoma esteso ai corpi ciliari, con rottura della membrana di Bruch e con infiltrazione sclerale ha prognosi pessima.
Trattamento
e risultati
L’evidenza
anatomica di un tumore completamente contenuto nel guscio sclerale e l'assenza
di vasi linfatici bulbari hanno giustificato per anni l'utilizzo
dell'enucleazione quale unica metodica terapeutica. Tuttavia, nonostante
l'apparente radicalità dell’intervento e l'assenza di metastasi al momento
del trattamento, l’analisi di ampie casistiche retrospettive evidenziava un
elevato tasso di mortalità: il 35% a 5 anni, il 57%
a 10 anni ed il 60% a 25 anni.
McLean e Zimmermann, in uno studio retrospettivo condotto su 3432 casi,
evidenziarono la presenza di un picco di mortalità a circa due anni
dall'intervento di enucleazione, dovuto forse ad una disseminazione di cellule
neoplastiche durante l'intervento chirurgico. Sulla base di questa ipotesi si
cercò di ridurre le conseguenze della manipolazione chirurgica del bulbo
oculare sottoponendolo a congelamento durante l'intervento,
o ad irradiazione, con
dose di 20 Gy, 24/48 ore prima dell'enucleazione.
Questi accorgimenti non hanno tuttavia dimostrato alcuna influenza sulla
prognosi quoad vitam del paziente enucleato. Vennero quindi sviluppate terapie
conservative in alternativa all'enucleazione (osservazione periodica di
piccole lesioni, trattamento laser, resezione chirurgica e radioterapia) in
grado di garantire al paziente, a parità di sopravvivenza, il mantenimento in
sede del bulbo oculare con un eventuale residuo visivo. L'osservazione
periodica viene riservata alle lesioni di piccole dimensioni (spessore
inferiore a 3mm) ed è giustificata dalla constatazione che alcune piccole
neoformazioni precedentemente classificate come melanomi a cellule fusate
erano in realta' nevi a cellule fusate. Inoltre sono stati documentati
melanomi a crescita zero, definiti "dormant melanoma" dagli Autori
anglosassoni, che non crescono e non metastatizzano. L'osservazione avviene
mediante valutazione oftalmoscopica ma soprattutto attraverso il confronto nel
tempo di fotografie seriate della lesione. Il trattamento fotocoagulativo
laser viene attualmente utilizzato solo per lesioni di piccole dimensioni (3mm
di spessore massimo) a sede periferica.
Le modalità di esecuzione variano dalla
fotocoagulazione transpupillare diretta con alte potenze, alla metodica Low
Energy-High Exposure introdotta allo scopo di aumentare la profondità della
necrosi. Il fascio di luce laser viene utilizzato per via transpupillare anche
nella terapia fotodinamica e nella termoterapia. La sopravvivenza dei pazienti
dopo questo tipo di trattamento appare sovrapponibile a quella ottenuta con le
metodiche più demolitive.
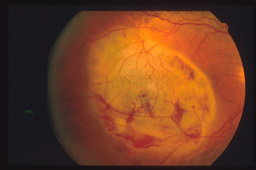
La
resezione chirurgica locale del tumore, introdotta da Foulds, comporta
l'asportazione del tumore dall'esterno. E' una tecnica chirurgica di difficile
esecuzione e limitata ai melanomi dei corpi ciliari e dell’iride. Il
trattamento conservativo del melanoma uveale attualmente più utilizzato è la
radioterapia. Lo scopo della radioterapia è quello di sterilizzare il tumore
inibendo la capacità replicativa cellulare.
Il melanoma uveale viene considerato radioresistente e per il suo trattamento
devono essere utilizzate dosi elevate di radiazioni (50-60 Gy), in genere mal
tollerate dalle strutture intraoculari più radiosensibili (cristallino, nervo
ottico, retina). Appare quindi indispensabile utilizzare tecniche di
irradiazione che consentano di somministrare alte dosi al tumore risparmiando
invece i tessuti peritumorali sani.
Già nel 1929 Moore tentò questo approccio
utilizzando una tecnica di brachiterapia interstiziale con aghi di Radon
impiantati direttamente nella massa neoplastica. Da allora ad oggi nuove e più
sofisticate metodiche sono state introdotte: la brachiterapia con placca
episclerale, la radioterapia con adroni (protoni e ioni elio) e la
radiochirurgia con Gamma Knife. La placca episclerale è costituita da un
guscio metallico di forma e dimensioni adeguate, contenente un isotopo
radioattivo (Cobalto 60, Rutenio 105, Iodio 125).
La placca viene suturata alla sclera in corrispondenza del tumore permanendo
il tempo necessario (sino a 10 giorni ) a somministrare una dose totale di
almeno 100 Gy. Grazie al guscio metallico l’irradiazione avviene
prevalentemente verso il tumore con una dispersione minima ai lati della
placchetta. Mediante questa tecnica possono essere trattate lesioni con
spessore massimo di 5mm. Il controllo locale di malattia è dell’85%, con
la conservazione di un buon grado di acuità visiva nella quasi totalità
dei pazienti. La radioterapia con adroni utilizza
generalmente protoni con energia di almeno 75 MV prodotti da un ciclotrone.
Le caratteristiche fisiche dei protoni (picco di Bragg) consentono di ottenere
un fascio molto collimato in grado di cedere tutta la dose terapeutica sul
bersaglio ad una profondità voluta. Presso
il Massachussets General Hospital-Harvard Cyclotron Laboratory di Boston, dal
1976 ad oggi, sono stati trattati oltre 2200 pazienti. La dose totale
somministrata è stata di 70 Gy equivalenti. L’analisi più recente è stata
condotta su 1006 casi ed è risultata in un controllo locale a 5 anni del 96%;
il 90% dei pazienti guariti ha conservato l’occhio, il 50%
l’acuità visiva. La sopravvivenza a 5 anni
è dell’80%.
Possono essere trattati tumori di tutte le
dimensioni ed in qualsiasi sede, ma i migliori risultati sono stati ottenuti
nelle lesioni con diametro inferiore a 16mm e spessore inferiore ad 8 mm che
interessavano la sola coroide. In qualche centro l’adroterapia è stata
praticata utilizzando ioni elio: è riportata una percentuale di fallimenti
locali assai bassa (2,4% a 5 anni
ed oltre), nettamente inferiore a quella ottenibile con altre forme di
irradiazione localizzata.
La Gamma Knife è una apparecchiatura complessa, che comprende, oltre l’unità
radiante, i sistemi per la localizzazione del tumore, la definizione del piano
di trattamento ed il controllo del trattamento. Il cuore della Gamma Knife è
un computer (Gamma Plan) direttamente interfacciato con i più sofisticati
sistemi di imaging neuroradiologici (tomografia computerizzata e risonanza
magnetica ad alta definizione). Sullo schermo del computer, al quale giungono
direttamente le immagini diagnostiche, l’operatore è quindi in grado di
localizzare il tumore, disegnarne i margini, individuare le parti anatomiche
da non irradiare, scegliere il collimatore di diametro adeguato alle
dimensioni del tumore, calcolare la dose di irradiazione (tempo per numero di
shot) ed infine visualizzare le isodosi del trattamento direttamente
sull’immagine neuroradiologica.

L'unità radiante contiene 201 sorgenti di
cobalto-60 collocate in un corpo emisferico centrale. Il raggio emesso da
ciascuna sorgente di cobalto viene accuratamente collimato e fatto convergere
con precisione in un punto comune, definito isocentro, corrispondente
all'intersezione dei raggi nel centro del casco collimatore. La distribuzione
geometrica delle sorgenti e il sistema di collimazione assicurano così dosi
elevate all’isocentro, di cui possono essere variate forma e dimensioni, con
risparmio dei tessuti perilesionali sani.
Le Mestastasi Oculari
Introduzione
Le metastasi uveali sono i tumori intraoculari più frequenti, anche se la
loro presenza è spesso sottostimata. Infatti, la valutazione autoptica di
bulbi oculari di pazienti deceduti per tumore ha evidenziato la presenza di
metastasi coroideali, clinicamente non rilevate in vita,
nel 4% dei casi.
L’uvea ha delle caratteristiche anatomiche peculiari. Infatti la sua
struttura vascolare è di tipo terminale a lobuli. Queste caratteristiche ne
fanno una specie di rete filtrante in cui eventuali cellule tumorali presenti
nel sangue, si impiantano e sviluppano
la metastasi.
Tumori
Primitivi
Al momento del riscontro di un secondarismo uveale la storia clinica di un
pregresso tumore primitivo è presente nel 70% dei casi. Nel restante 30% non
vi è invece un’anamnesi positiva per patologie tumorali pregresse.
In questi pazienti una successiva valutazione oncologica sistemica rivela la
presenza del tumore primitivo solo nel 50% dei casi.
Quindi nel 17% dei pazienti in cui viene diagnosticata una metastasi uveale,
non si riesce ad individuare la sede del tumore primitivo da cui è
originata.
I tumori che più frequentemente
determinano metastasi coroideali sono i carcinomi. I più frequenti sono il
tumore della mammella (47%), del polmone (21%), del tratto gastrointestinale
(4%), del rene (2%), della pelle (2%), della prostata (2%), altre sedi (4%) e
sede sconosciuta (17%).
Le donne rappresentano il 70% dei pazienti affetti da secondarismi uveali in
virtù dello spiccato tropismo per la coroide che ha il carcinoma della
mammella.
L’età media dei pazienti è tra i 40 ed i 70 anni e dipende dalle
caratteristiche epidemiologiche del tumore di origine.
Caratteristiche Cliniche
La
sede più frequente delle metastasi uveali è la coroide (90%), i corpi
ciliari sono interessati nel 20% e l’iride nel 10%. La lesione è infatti
unica nel 70% dei casi mentre nel
restante 30% può essere multifocale.
La
metastasi uveale può presentarsi bilateralmente circa nel 30% dei casi.
La multifocalità e la bilateralità rappresentano due caratteristiche
patognomonica di secondarismo molto utili nella diagnosi differenziale.
La localizzazione sottomaculare è presente nel 12% dei casi, mentre
nell’80% la sede è tra macula ed equatore.
Solamente l’8% delle metastasi sono post equatoriali.
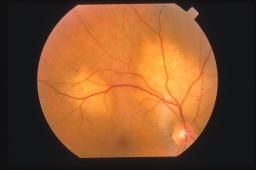
Oftalmoscopicamente la metastasi si presenta come una lesione giallastra con
una forma placoide. Lo spessore medio ecografico è di 3mm ed il diametro
medio è di circa 9mm.
Nelle lesioni più spesse vi è un distacco sieroso della retina sovrastante
la massa con alterazioni dell’epitelio pigmentato retinico. Questo tipo di
alterazione accompagna le metastasi nel 75% dei casi.
Diagnosi differenziale
La
diagnosi di metastasi coroideale è solamente clinica e si basa principalmente
su un’anamnesi clinica positiva per tumore primitivo e sulle caratteristiche
morfologiche della lesione.
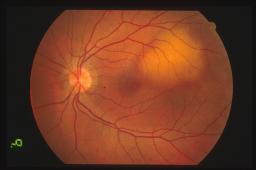
La
diagnosi differenziale di una metastasi è verso altre lesione amenalnotiche
uveali che in ordine di frequenza sono: il melanoma amelanotico, l’emangioma
coroideale, il nevo amelanotico coroideale, sclerite posteriore, osteoma
coroideale, infiammazioni corioretiniche granulomatose e più raramente
degenerazioni maculari essudative.
Gli esami oftalmologici strumentali (ecografia oculare, fluorangiografia
retinica, angiografia con verde indocianina) possono fornire indicazioni tra
loro complementari sull’aspetto morfologico della lesione. Tali parametri
tuttavia servono più a escludere certe patologie più che a essere
patognomoniche di metastasi.
Anche l’assenza di un tumore primitivo alla diagnosi e addirittura dopo la
valutazione sistemica oncologica non esclude la natura metastatica della
lesione uveale.
Trattamento
Se
il tumore era misconosciuto il trattamento iniziale riguarderà il tumore
primitivo e successivamente, in funzione della prognosi quoad vitam, la
metastasi oculare. Se il tumore è noto il trattamento sarà sistemico e
locale.
Infatti lo scopo della terapia è quello di sterilizzare la metastasi
coroideale, in modo che essa stessa non determini ulteriori disseminazioni per
via ematogena, e distruggere eventuali metastasi sub cliniche sistemiche.
Questo obiettivo viene perseguito con un primo approccio chemioterapico
sistemico. Se non c’è risposta terapeutica adeguata alla chemioterapia o la
lesione è a sede sottomaculare si deve utilizzare la radioterapia esterna
(3000-4000 cGy) con dosi iperfrazionate allo scopo di ridurre al minimo gli
effetti collaterali comunque inevitabili nel tempo.
Prognosi
In
genere la prognosi per questi pazienti non è buona con una sopravvivenza
media di 18 mesi dalla diagnosi. Tuttavia le pazienti con carcinoma della
mammella presentano una prognosi quoad vitam migliore soprattutto se la
metastasi coroideale era solitaria e prontamente trattata.